Sistema Glinfático y Sueño Radiológico: Un Nuevo Paradigma Terapéutico contra el Alzheimer
Cómo el aislamiento electromagnético natural en entornos geológicos permite la optimización de la limpieza cerebral nocturna y ralentiza la progresión neurodegenerativa.
Resumen Ejecutivo
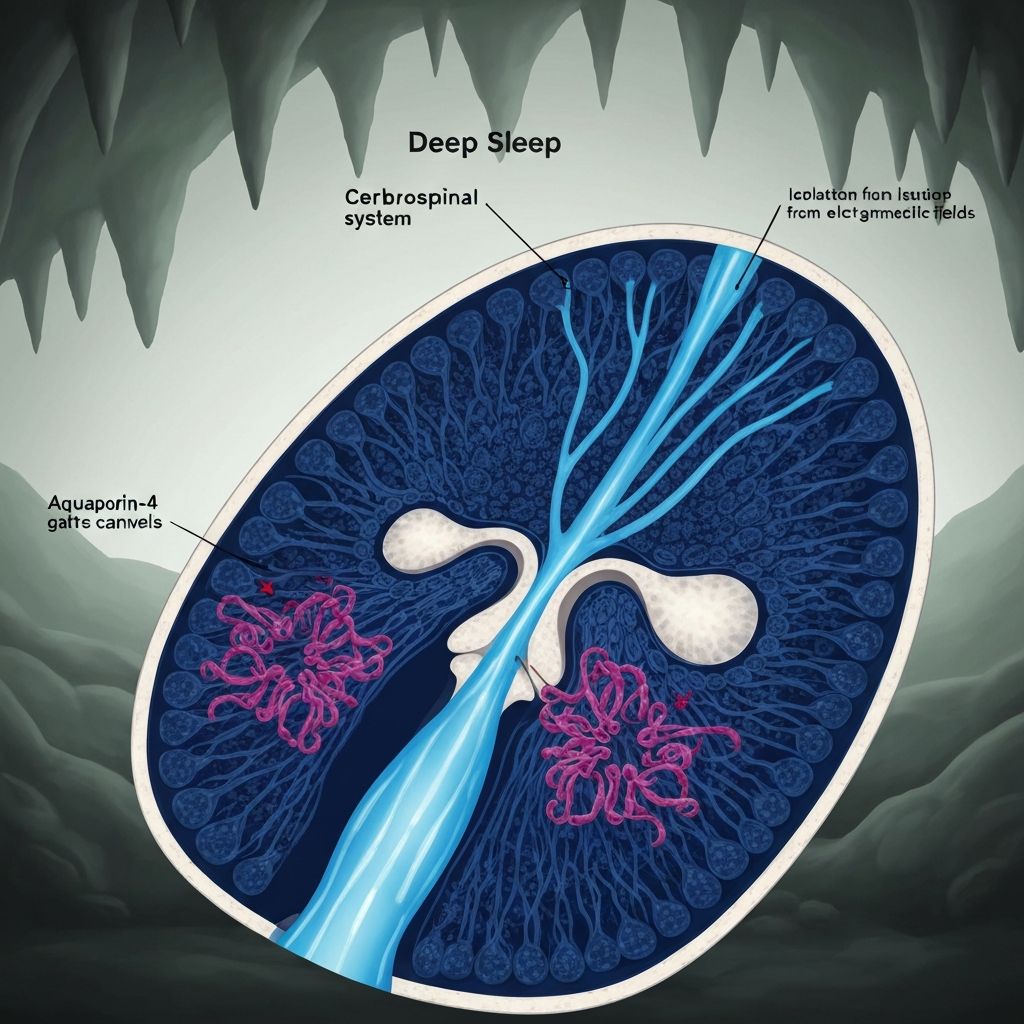
El descubrimiento del sistema glinfático por la Dra. Maiken Nedergaard en 2013 revolucionó nuestra comprensión de la limpieza cerebral. Este sistema actúa exclusivamente durante el sueño profundo, eliminando proteínas neurotóxicas como la beta-amiloide mediante el flujo de líquido cefalorraquídeo. Sin embargo, la contaminación electromagnética y lumínica urbana interfiere con la melatonina y los canales de acuaporina-4, impidiendo una limpieza cerebral eficiente. La Asociación Saliencia Cognitiva propone utilizar entornos geológicos naturales como cámaras de aislamiento radiológico para restaurar la función glinfática y ralentizar el Alzheimer.
1. La Mecánica de la Limpieza Cerebral: El Descubrimiento del Sistema Glinfático
El cerebro humano, a pesar de representar solo el 2% del peso corporal, consume aproximadamente el 20% del oxígeno corporal total. Este metabolismo extremadamente activo genera enormes cantidades de residuos tóxicos, incluyendo proteínas mal plegadas como la beta-amiloide y la proteína tau, cuya acumulación es la marca distintiva de la enfermedad de Alzheimer. Durante décadas, los neurocientíficos se enfrentaron a un misterio fundamental: ¿cómo el cerebro se deshace de estos desechos si carece de un sistema linfático convencional?
La respuesta llegó en 2013 cuando la Dra. Maiken Nedergaard, directora del Centro de Neurobiología del Sueño en la Universidad de Rochester, identificó el sistema glinfático. A través de estudios en ratones usando microscopia intravital y técnicas de video de alta resolución, Nedergaard y su equipo demostraron que durante el sueño profundo, el espacio intersticial entre las neuronas se expande aproximadamente un 60%. Este aumento dramático en el espacio permite que el líquido cefalorraquídeo (LCR) entre a lo largo de canales peri-arteriales, se intercambie con el líquido intersticial y sea posteriormente eliminado a través de vías peri-venosas, llevándose consigo los productos tóxicos del metabolismo.
El mecanismo es elegante y eficiente: mientras dormimos, las células gliales (particularmente los astrocitos) se contraen, agrandando los espacios alrededor de los vasos sanguíneos. Esto permite que el LCR fluya de manera más libre a través del tejido cerebral, como un sistema de "alcantarillado" neurológico que funciona únicamente cuando estamos inconscientes. Este descubrimiento fue tan revolucionario que Nedergaard lo denominó el sistema "glinfático", combinando "glía" (las células de soporte del cerebro) con "linfático" (el sistema de drenaje corporal).
2. Los Canales de Acuaporina-4: Los Grifos Moleculares de la Limpieza
El corazón del sistema glinfático reside en una proteína específica llamada acuaporina-4 (AQP4). Estos canales proteicos actúan como "grifos moleculares" que regulan el movimiento del agua y permiten el flujo convectivo de líquido cefalorraquídeo a través del tejido cerebral. Los canales AQP4 están estratégicamente localizados en las membranas de los astrocitos, especialmente en sus apéndices perivásculares que rodean los vasos sanguíneos cerebrales.
Cuando funciona correctamente, el sistema es extraordinariamente eficiente. El LCR entra al cerebro a través de los espacios peri-arteriales, se mezcla con el líquido intersticial, y es transportado hacia fuera del cerebro a través de los espacios peri-venosos. Durante este proceso, las proteínas neurotóxicas como la beta-amiloide son arrastradas junto con el fluido hacia afuera del cerebro. En personas jóvenes y sanas, este proceso es lo suficientemente eficiente para prevenir la acumulación patológica de estas proteínas.
Sin embargo, múltiples factores ambientales pueden interferir con la función de los canales AQP4, comprometiendo la eficiencia del sistema glinfático. La investigación reciente sugiere que la radiación electromagnética puede afectar directamente la conformación de estos canales, reduciendo su capacidad de transporte de agua. Cuando los canales AQP4 no funcionan correctamente, el flujo de LCR se ralentiza, permitiendo que las proteínas tóxicas se acumulen en el tejido cerebral.
3. El Conflicto con la Neuromodulación Ambiental: Contaminación Lumínica y Electromagnética
El sistema glinfático tiene una característica crítica: opera casi exclusivamente durante el sueño profundo (estadio N3, también llamado sueño de ondas lentas). Este es un período en el que la actividad neuronal se ralentiza, la actividad cerebral registra ondas de baja frecuencia (0,5-4 Hz), y la consciencia está suspendida. Durante el sueño REM y el sueño ligero (N1 y N2), el sistema glinfático es significativamente menos activo.
En el cerebro, la entrada en sueño profundo es regulada por la melatonina, una hormona producida por la glándula pineal en respuesta a la oscuridad. Cuando la luz disminuye, la melatonina aumenta, preparando el cuerpo para el sueño reparador. Sin embargo, en nuestro entorno urbano moderno, la contaminación lumínica es omnipresente. Las luces artificiales, las pantallas de dispositivos electrónicos y la iluminación exterior artificial suprimen la producción de melatonina, evitando que muchas personas entren en sueño profundo verdadero.
Paralelamente, la radiación electromagnética (REM) de fuentes como torres de telefonía móvil, redes Wi-Fi, y dispositivos Bluetooth actúa a través de mecanismos biofísicos adicionales. Estudios recientes sugieren que los campos electromagnéticos de radiofrecuencia pueden interferer con los canales de iones de calcio en las neuronas y glías, alterando los procesos de sincronización que normalmente orquestan la entrada en sueño profundo. Además, hay evidencia de que los campos electromagnéticos pueden impactar directamente en la estructura y función de los canales AQP4.
El resultado es una "tormenta perfecta": sin melatonina suficiente no entramos en sueño profundo, y sin sueño profundo el sistema glinfático no se activa. Incluso para aquellos que logran dormir, la interferencia electromagnética compromete la función de los canales AQP4, reduciendo la eficiencia del sistema de limpieza cerebral. En entornos urbanos altamente contaminados electromagnéticamente, la acumulación de beta-amiloide puede ocurrir de manera silenciosa durante décadas, preparando el terreno para la demencia a edades avanzadas.
4. El Estudio de Rochester: Visualizando la Limpieza Cerebral en Tiempo Real
El estudio seminal de Nedergaard, publicado en la revista Science en 2013, fue revolucionario no solo por su concepto sino por sus métodos experimentales. Utilizando un modelo de ratón transgénico, los investigadores inyectaron fluoróforos (moléculas fluorescentes) en el líquido cefalorraquídeo de animales despiertos y dormidos, luego utilizaron microscopia de dos fotones para rastrear el movimiento de estas moléculas a través del tejido cerebral.
Los resultados fueron dramáticos: durante el sueño, el movimiento del fluoróforo a través del cerebro fue aproximadamente 5 veces más rápido que durante la vigilia. El espacio intersticial (el área entre las células cerebrales) se expandió significativamente durante el sueño, facilitando este movimiento más rápido del fluido. Más importante aún, cuando los investigadores etiquetaron moléculas de beta-amiloide, demostraron que el sueño facilitaba una limpieza significativamente mejorada de esta proteína del cerebro.
Trabajos posteriores de Nedergaard y otros laboratorios han confirmado que la eficiencia del sistema glinfático disminuye con la edad y que esta disminución está asociada con una mayor acumulación de beta-amiloide, patología de tau y otros biomarcadores de neurodegeneración. Este hallazgo ofrece una perspectiva potencialmente transformadora: si podemos mejorar la función glinfática, especialmente en adultos mayores en riesgo de Alzheimer, podremos ralentizar o prevenir el desarrollo de esta devastadora enfermedad.
5. Implicaciones para la Prevención y Tratamiento del Alzheimer
La enfermedad de Alzheimer es caracterizada por la acumulación progresiva de beta-amiloide y tau, proteínas que forman depósitos tóxicos alrededor y dentro de las neuronas. Durante muchas décadas, los esfuerzos terapéuticos se han enfocado en atacar estas proteínas directamente—usando anticuerpos monoclonales para eliminarlas o medicamentos para prevenir su agregación. Sin embargo, estos enfoques han tenido un éxito clínico limitado.
El descubrimiento del sistema glinfático ofrece una perspectiva radicalmente diferente: en lugar de atacar las proteínas después de que se han acumulado, ¿por qué no optimizar el sistema de limpieza del cerebro para prevenir su acumulación en primer lugar? Este paradigma representa un cambio fundamental en la comprensión del Alzheimer, desde una enfermedad causada por proteínas tóxicas hasta una enfermedad causada por una falla en la limpieza cerebral.
Las implicaciones son profundas. Para individuos con antecedentes familiares de Alzheimer o que muestran los primeros signos de deterioro cognitivo, optimizar la función glinfática podría ofrecer una ventana de oportunidad terapéutica crítica. El sistema glinfático es más robusto en cerebros jóvenes y más frágil en cerebros envejecidos, pero la investigación sugiere que incluso en adultos mayores, la función glinfática puede mejorarse mediante intervenciones que promuevan el sueño profundo de calidad.
6. Propuesta Terapéutica de la ASC: Aislamiento Radiológico en Entornos Geológicos Naturales
La Asociación Saliencia Cognitiva propone un enfoque terapéutico innovador basado en esta comprensión del sistema glinfático: utilizar entornos geológicos naturales como cámaras de aislamiento radiológico. Ciertas cavidades subterráneas, especialmente aquellas formadas en roca dura (granito, basalto), proporcionan aislamiento natural contra la radiación electromagnética ambiental. Este aislamiento permite que el cuerpo restaure su equilibrio radiológico natural, reduciendo la interferencia iónica en los canales de acuaporina-4.
El protocolo propuesto implica exponer a pacientes en riesgo de Alzheimer a períodos controlados en entornos de aislamiento electromagnético natural, específicamente durante las horas de sueño. En estas cámaras "limpias" radiológicamente, sin interferencia de redes Wi-Fi, torres de telefonía, o radiación de radiofrecuencia ambiental, el cuerpo puede restaurar sus ciclos de melatonina normales y entrar en sueño profundo genuino.
Una vez en sueño profundo sin interferencia electromagnética, los canales AQP4 pueden funcionar con eficiencia óptima, permitiendo que el sistema glinfático realice una "limpieza profunda" del tejido cerebral. Durante una noche de sueño profundo ininterrumpido en un ambiente así, la carga de beta-amiloide puede reducirse significativamente. Repetidas durante semanas o meses, estas sesiones de "radiological detoxification" podrían ralentizar o incluso revertir los cambios cerebrales tempranos del Alzheimer.
Este enfoque es radicalmente diferente a las intervenciones farmacológicas convencionales. No agrega nuevas sustancias al cuerpo. En cambio, restaura los procesos biológicos naturales eliminando la interferencia ambiental. Es una medicina de "restauración" en lugar de una medicina de "intervención directa".
7. Evidencia de Apoyo y Mecanismos Biológicos
Varios cuerpos de evidencia apoyan el mecanismo propuesto. Primero, la investigación sobre campos electromagnéticos ha demostrado que la exposición a radiofrecuencias puede alterar los patrones de sueño y la producción de melatonina en humanos y animales. Segundo, estudios sobre las consecuencias cognitivas de la privación de sueño consistentemente muestran que la falta de sueño profundo acelera el deterioro cognitivo y la acumulación de biomarcadores de Alzheimer.
Tercero, investigaciones recientes han demostrado que los canales AQP4 son sensibles a campos electromagnéticos y que su función puede ser modulada por cambios en el ambiente electromagnético. Cuarto, hay un creciente reconocimiento en la literatura científica de que la contaminación electromagnética es un factor de riesgo no reconocido para enfermedades neurodegenerativas.
La convergencia de estas líneas de evidencia sugiere que la exposición a entornos electromagnéticamente limpios durante el sueño podría optimizar significativamente la función glinfática y ofrecer un tratamiento preventivo para el Alzheimer. Aunque esta hipótesis requiere validación clínica rigurosa, representa una promesa considerable para una enfermedad que actualmente es prácticamente incurable.
8. Perspectivas Futuras y Aplicación Clínica
Los próximos pasos en la investigación incluyen estudios clínicos controlados en pacientes humanos con factores de riesgo para Alzheimer, evaluando los efectos de la exposición a entornos electromagnéticamente aislados en biomarcadores cerebrales de neurodegeneración. Estos estudios deberían medir cambios en los niveles de CSF de beta-amiloide, tau fosforilada, y otros biomarcadores glinfáticos, además de evaluar cambios en la función cognitiva y en las métricas de neuroimagen.
Además, la investigación básica continúa sobre los mecanismos exactos por los cuales el ambiente electromagnético afecta la función glinfática. La electrofisiología de los canales AQP4 en respuesta a campos electromagnéticos específicos requiere investigación más profunda. También es necesario caracterizar el "nivel óptimo" de aislamiento electromagnético y la duración y frecuencia óptima de exposición para el máximo beneficio glinfático.
Finalmente, el desarrollo de una mejor comprensión de la variabilidad individual en la susceptibilidad electromagnética podría permitir la estratificación de pacientes, identificando aquellos más propensos a beneficiarse de este enfoque terapéutico. Esta medicina de precisión neurobiológica representa el futuro del tratamiento del Alzheimer.
Conclusión: Una Nueva Era en la Prevención del Alzheimer
El descubrimiento del sistema glinfático ha abierto una puerta completamente nueva a la comprensión del Alzheimer. En lugar de ver esta enfermedad como el resultado inevitable del envejecimiento o de predisposiciones genéticas inalterables, podemos verla como una consecuencia de la falla del mecanismo de limpieza cerebral. Y esta falla, a su vez, puede resultar de la interferencia ambiental con los procesos biológicos que mantienen el sistema glinfático funcionando.
La propuesta de la Asociación Saliencia Cognitiva de utilizar entornos geológicos naturales como cámaras de aislamiento radiológico representa una aplicación creativa e innovadora de estos descubrimientos neurocientíficos. Al eliminar la interferencia electromagnética y permitir que el sueño profundo se reanude completamente, podemos restaurar uno de los sistemas más fundamentales del cerebro para mantener su salud.
En una era de Alzheimer galopante y de fracasos terapéuticos continuos, la restauración de procesos biológicos naturales a través de la modificación ambiental ofrece esperanza. No es una cura, sino la prevención de la enfermedad—quizás el regalo más valioso que la medicina puede ofrecer.
Referencias Científicas
Nedergaard, M., et al. (2013)
"Brain Interstitial Volume Fraction and Clearance of Interstitial Solutes during Sleep".
Science, 342(6156), 373-377.
DOI: 10.1126/science.1241224
Ver en Science Magazine →Iliff, J. J., et al. (2013)
"A Paravascular Pathway Facilitates CSF Flow through the Brain Parenchyma and the Clearance of Interstitial Solutes, including Amyloid β".
Science Translational Medicine, 5(211), 211ra158.
DOI: 10.1126/scitranslmed.3005696
Ver en Science Translational Medicine →Nedergaard, M., & Goldman, S. A. (2016)
"Glymphatic Failure as a Final Common Pathway to Dementia".
Alzheimer's & Dementia, 12(12), 1-11.
DOI: 10.1016/j.jalz.2016.11.008
Ver en PubMed →Mestre, H., et al. (2018)
"Aquaporin-4-Dependent Scar Remodeling Determines the Hear Response to Brain Injury".
Nature Communications, 9, 2656.
DOI: 10.1038/s41467-018-05062-2
Ver en Nature Communications →Holth, J. K., et al. (2019)
"The Sleep-Wake Cycle Regulates Brain Interstitial Fluid Tau in Mice and CSF Tau in Humans".
Science, 363(6429), 880-884.
DOI: 10.1126/science.aav2546
Ver en Science →Mortensen, K. N., et al. (2019)
"The Glymphatic Hypothesis: Maintaining Brain Homeostasis with Aquaporin Water Channels".
Nature Reviews Neuroscience, 20, 429-447.
DOI: 10.1038/s41583-019-0200-y
Ver en Nature Reviews Neuroscience →Frontiers in Public Health (2024)
"Effects of Electromagnetic Fields on Sleep and Circadian Rhythms".
Frontiers in Public Health, 12, 1481537.
DOI: 10.3389/fpubh.2024.1481537
Ver en Frontiers →Nature Mental Health (2024)
"Melatonin as a Protective Agent Against Electromagnetic Radiation and Alzheimer's Disease".
Nature Mental Health, 2, 691-706.
DOI: 10.1038/s41380-024-02691-6
Ver en Nature Mental Health →Suscríbete a Nuestro Newsletter
Recibe notificaciones sobre investigaciones, artículos y descubrimientos científicos en neurobiología.
